Kvantová mechanika ti pomůže pochopit, jak fungují atomy na nejzákladnější... Zobrazit více
Registruj se, abys viděl obsahJe to zdarma!
Přístup ke všem dokumentům
Zlepši své známky
Připoj se k milionům studentů
Knowunity AI
Předměty
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Zobrazit všechna témata
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Zobrazit všechna témata
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Zobrazit všechna témata
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Zobrazit všechna témata
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Zobrazit všechna témata
158
•
Aktualizováno Mar 28, 2026
•
Nikol Schneiderová
@nikolschneidero
Kvantová mechanika ti pomůže pochopit, jak fungují atomy na nejzákladnější... Zobrazit více

Kvantová mechanika je nejpřesnější způsob, jak popsat stavbu atomu. Energie se nemění plynule jako voda z kohoutku, ale skáče po větších částech - kvantech. Je to trochu jako chůze po schodech místo jízdy po šikmé ploše.
Každý elektron v atomu popisujeme pomocí čtyř kvantových čísel. Představ si to jako adresu - každý elektron má svou unikátní kombinaci těchto čísel, která určuje jeho vlastnosti i chování.
Hlavní kvantové číslo (n) ti říká, jak daleko od jádra se elektron nachází. Může nabývat hodnot n1, n2... až n8 (nebo K, L, M... R). Čím vyšší číslo, tím dál od jádra elektron krouží.
Orbital není dráha jako u planety, ale spíš "oblak pravděpodobnosti" - prostor, kde se elektron nejspíš nachází. Elektron se v něm může volně pohybovat, přesnou polohu nikdy neznáme.
💡 Tip: Hlavní kvantové číslo často odpovídá číslu periody v periodické tabulce!
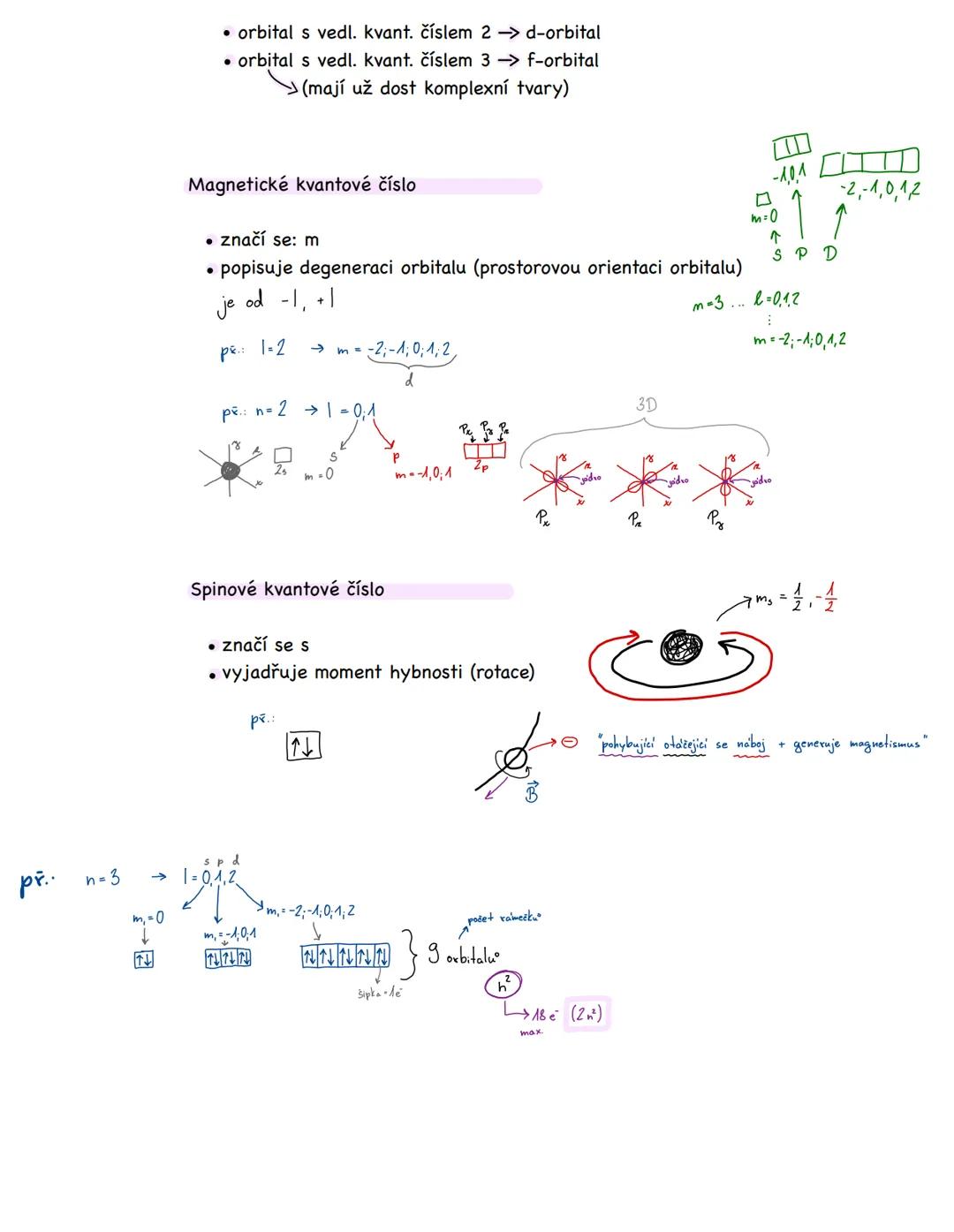
Vedlejší kvantové číslo (l) určuje tvar orbitalu a nabývá hodnot od 0 do n-1. Každému číslu odpovídá jiný typ: l=0 je s-orbital, l=1 je p-orbital, l=2 je d-orbital a l=3 je f-orbital. Čím vyšší číslo, tím složitější tvar.
Magnetické kvantové číslo (m) popisuje prostorovou orientaci orbitalu - kam v prostoru "míří". Pohybuje se od -l do +l. Například pro d-orbitaly může být m = -2, -1, 0, 1, 2, což znamená pět různých orientací.
Spinové kvantové číslo (s) vyjadřuje rotaci elektronu kolem vlastní osy. Můžeš si to představit jako šipky ↑ a ↓ - elektron se může točit "nahoru" nebo "dolů". V jednom orbitalu mohou být maximálně dva elektrony s opačnými spiny.
💡 Zapamatuj si: Počet orbitalů = 2n², kde n je hlavní kvantové číslo. Pro n=3 máš 18 možných pozic pro elektrony!
Náš AI společník je speciálně vytvořen pro potřeby studentů. Na základě milionů obsahových materiálů, které máme na platformě, můžeme studentům poskytovat opravdu smysluplné a relevantní odpovědi. Ale nejde jen o odpovědi, společník je ještě více o provázení studentů jejich každodenními výzvami v učení, s personalizovanými studijními plány, kvízy nebo obsahovými materiály v chatu a 100% personalizací na základě dovedností a vývoje studentů.
Aplikaci si můžete stáhnout z obchodu Google Play a Apple App Store.
Ano, máte bezplatný přístup k obsahu v aplikaci a k našemu společníkovi s umělou inteligencí. Chcete-li odemknout určité funkce aplikace, můžete si zakoupit aplikaci Knowunity Pro.
App Store
Google Play
Aplikace je velmi jednoduchá na používání a dobře navržená. Zatím jsem našel vše, co jsem hledal, a mohl jsem se z prezentací hodně naučit! Určitě použiju aplikaci na školní úkol! A samozřejmě taky hodně pomáhá jako inspirace.
Stefan S
uživatel iOS
Tahle aplikace je fakt skvělá. Je tam tolik studijních poznámek a pomůcek [...]. Můj problémový předmět je například francouzština a aplikace nabízí tolik možností pomoci. Díky této aplikaci jsem si zlepšil francouzštinu. Doporučil bych ji každému.
Samantha Klich
uživatelka Androidu
Páni, jsem opravdu ohromen. Zkusil jsem aplikaci jen proto, že jsem ji mnohokrát viděl v reklamách, a byl jsem naprosto ohromen. Tato aplikace je TA POMOC, kterou chceš do školy, a především nabízí spoustu věcí, jako jsou cvičení a přehledy faktů, které mi osobně VELMI pomohly.
Anna
uživatelka iOS
Dříve jsem měl problémy s dokončováním úkolů včas, dokud jsem neobjevil Knowunity, který nejen usnadňuje nahrávání mého vlastního obsahu, ale také poskytuje skvělé shrnutí, díky kterým je moje práce rychlejší a efektivnější.
Thomas R
uživatel iOS
Vždy bylo výzvou najít všechny důležité informace pro mé úkoly – od té doby, co používám Knowunity, můžu jednoduše nahrát svůj obsah a těžit ze shrnutí ostatních, což mi hodně pomáhá s organizací.
Lisa M
uživatelka Androidu
Často jsem měl pocit, že nemám dostatečný přehled při učení, ale od té doby, co používám Knowunity, to už neplatí – nahraju svůj obsah a vždy najdu užitečná shrnutí na platformě, což mi učení značně usnadňuje.
David K
uživatel iOS
Ta aplikace je prostě skvělá! Stačí zadat téma do vyhledávání a dostanu odpověď opravdu rychle. Nemusím koukat na 10 YouTube videí, abych něčemu porozuměl, takže šetřím čas. Vřele doporučuji!
Sudenaz Ocak
uživatel Androidu
Ve škole mi matematika vůbec nešla, ale díky této aplikaci se mi teď daří lépe. Jsem moc vděčný, že jste tuhle aplikaci vytvořili.
Greenlight Bonnie
uživatel Androidu
Dřív bylo opravdu těžké shromáždit všechny informace na moje prezentace. Ale od té doby, co používám Knowunity, prostě nahraju svoje poznámky a najdu skvělé souhrny od ostatních – díky tomu je moje studium mnohem efektivnější!
Julia S
uživatelka Androidu
Byl jsem neustále ve stresu kvůli všem studijním materiálům, ale od té doby, co používám Knowunity, nahrávám svoje věci a koukám na super souhrny od ostatních – opravdu mi to pomáhá všechno lépe zvládat a je to mnohem méně stresující.
Marco B
uživatel iOS
TY KVÍZY A KARTIČKY SOU TAK UŽITEČNÝ A MILUJU Knowunity AI. JE TO TAKY DOSLOVA JAKO CHATGPT ALE CHYTŘEJŠÍ!! POMOHLO MI TO I S PROBLÉMY S ŘASENKOU!! A TAKY S MÝMA SKUTEČNÝMA PŘEDMĚTAMA! JASNÝ 😍😁😲🤑💗✨🎀😮
Sarah L
uživatelka Androidu
Dřív jsem trávil hodiny googlováním školních materiálů, ale teď prostě nahraju svoje věci na Knowunity a prohlížím si užitečné souhrny od ostatních – při přípravě na zkoušky se cítím mnohem jistější.
Paul T
uživatel iOS
Aplikace je velmi jednoduchá na používání a dobře navržená. Zatím jsem našel vše, co jsem hledal, a mohl jsem se z prezentací hodně naučit! Určitě použiju aplikaci na školní úkol! A samozřejmě taky hodně pomáhá jako inspirace.
Stefan S
uživatel iOS
Tahle aplikace je fakt skvělá. Je tam tolik studijních poznámek a pomůcek [...]. Můj problémový předmět je například francouzština a aplikace nabízí tolik možností pomoci. Díky této aplikaci jsem si zlepšil francouzštinu. Doporučil bych ji každému.
Samantha Klich
uživatelka Androidu
Páni, jsem opravdu ohromen. Zkusil jsem aplikaci jen proto, že jsem ji mnohokrát viděl v reklamách, a byl jsem naprosto ohromen. Tato aplikace je TA POMOC, kterou chceš do školy, a především nabízí spoustu věcí, jako jsou cvičení a přehledy faktů, které mi osobně VELMI pomohly.
Anna
uživatelka iOS
Dříve jsem měl problémy s dokončováním úkolů včas, dokud jsem neobjevil Knowunity, který nejen usnadňuje nahrávání mého vlastního obsahu, ale také poskytuje skvělé shrnutí, díky kterým je moje práce rychlejší a efektivnější.
Thomas R
uživatel iOS
Vždy bylo výzvou najít všechny důležité informace pro mé úkoly – od té doby, co používám Knowunity, můžu jednoduše nahrát svůj obsah a těžit ze shrnutí ostatních, což mi hodně pomáhá s organizací.
Lisa M
uživatelka Androidu
Často jsem měl pocit, že nemám dostatečný přehled při učení, ale od té doby, co používám Knowunity, to už neplatí – nahraju svůj obsah a vždy najdu užitečná shrnutí na platformě, což mi učení značně usnadňuje.
David K
uživatel iOS
Ta aplikace je prostě skvělá! Stačí zadat téma do vyhledávání a dostanu odpověď opravdu rychle. Nemusím koukat na 10 YouTube videí, abych něčemu porozuměl, takže šetřím čas. Vřele doporučuji!
Sudenaz Ocak
uživatel Androidu
Ve škole mi matematika vůbec nešla, ale díky této aplikaci se mi teď daří lépe. Jsem moc vděčný, že jste tuhle aplikaci vytvořili.
Greenlight Bonnie
uživatel Androidu
Dřív bylo opravdu těžké shromáždit všechny informace na moje prezentace. Ale od té doby, co používám Knowunity, prostě nahraju svoje poznámky a najdu skvělé souhrny od ostatních – díky tomu je moje studium mnohem efektivnější!
Julia S
uživatelka Androidu
Byl jsem neustále ve stresu kvůli všem studijním materiálům, ale od té doby, co používám Knowunity, nahrávám svoje věci a koukám na super souhrny od ostatních – opravdu mi to pomáhá všechno lépe zvládat a je to mnohem méně stresující.
Marco B
uživatel iOS
TY KVÍZY A KARTIČKY SOU TAK UŽITEČNÝ A MILUJU Knowunity AI. JE TO TAKY DOSLOVA JAKO CHATGPT ALE CHYTŘEJŠÍ!! POMOHLO MI TO I S PROBLÉMY S ŘASENKOU!! A TAKY S MÝMA SKUTEČNÝMA PŘEDMĚTAMA! JASNÝ 😍😁😲🤑💗✨🎀😮
Sarah L
uživatelka Androidu
Dřív jsem trávil hodiny googlováním školních materiálů, ale teď prostě nahraju svoje věci na Knowunity a prohlížím si užitečné souhrny od ostatních – při přípravě na zkoušky se cítím mnohem jistější.
Paul T
uživatel iOS
Nikol Schneiderová
@nikolschneidero
Kvantová mechanika ti pomůže pochopit, jak fungují atomy na nejzákladnější úrovni. Místo plynulých změn energie se všechno děje po menších "balíčcích" zvaných kvanta, což vysvětluje mnoho záhad atomového světa.

Přístup ke všem dokumentům
Zlepši své známky
Připoj se k milionům studentů
Kvantová mechanika je nejpřesnější způsob, jak popsat stavbu atomu. Energie se nemění plynule jako voda z kohoutku, ale skáče po větších částech - kvantech. Je to trochu jako chůze po schodech místo jízdy po šikmé ploše.
Každý elektron v atomu popisujeme pomocí čtyř kvantových čísel. Představ si to jako adresu - každý elektron má svou unikátní kombinaci těchto čísel, která určuje jeho vlastnosti i chování.
Hlavní kvantové číslo (n) ti říká, jak daleko od jádra se elektron nachází. Může nabývat hodnot n1, n2... až n8 (nebo K, L, M... R). Čím vyšší číslo, tím dál od jádra elektron krouží.
Orbital není dráha jako u planety, ale spíš "oblak pravděpodobnosti" - prostor, kde se elektron nejspíš nachází. Elektron se v něm může volně pohybovat, přesnou polohu nikdy neznáme.
💡 Tip: Hlavní kvantové číslo často odpovídá číslu periody v periodické tabulce!

Přístup ke všem dokumentům
Zlepši své známky
Připoj se k milionům studentů
Vedlejší kvantové číslo (l) určuje tvar orbitalu a nabývá hodnot od 0 do n-1. Každému číslu odpovídá jiný typ: l=0 je s-orbital, l=1 je p-orbital, l=2 je d-orbital a l=3 je f-orbital. Čím vyšší číslo, tím složitější tvar.
Magnetické kvantové číslo (m) popisuje prostorovou orientaci orbitalu - kam v prostoru "míří". Pohybuje se od -l do +l. Například pro d-orbitaly může být m = -2, -1, 0, 1, 2, což znamená pět různých orientací.
Spinové kvantové číslo (s) vyjadřuje rotaci elektronu kolem vlastní osy. Můžeš si to představit jako šipky ↑ a ↓ - elektron se může točit "nahoru" nebo "dolů". V jednom orbitalu mohou být maximálně dva elektrony s opačnými spiny.
💡 Zapamatuj si: Počet orbitalů = 2n², kde n je hlavní kvantové číslo. Pro n=3 máš 18 možných pozic pro elektrony!
Náš AI společník je speciálně vytvořen pro potřeby studentů. Na základě milionů obsahových materiálů, které máme na platformě, můžeme studentům poskytovat opravdu smysluplné a relevantní odpovědi. Ale nejde jen o odpovědi, společník je ještě více o provázení studentů jejich každodenními výzvami v učení, s personalizovanými studijními plány, kvízy nebo obsahovými materiály v chatu a 100% personalizací na základě dovedností a vývoje studentů.
Aplikaci si můžete stáhnout z obchodu Google Play a Apple App Store.
Ano, máte bezplatný přístup k obsahu v aplikaci a k našemu společníkovi s umělou inteligencí. Chcete-li odemknout určité funkce aplikace, můžete si zakoupit aplikaci Knowunity Pro.
6
Chytré Nástroje NOVÉ
Přeměň tyto poznámky na: ✓ 50+ Cvičných Otázek ✓ Interaktivní Kartičky ✓ Úplný zkušební test ✓ Osnovy Esejů
App Store
Google Play
Aplikace je velmi jednoduchá na používání a dobře navržená. Zatím jsem našel vše, co jsem hledal, a mohl jsem se z prezentací hodně naučit! Určitě použiju aplikaci na školní úkol! A samozřejmě taky hodně pomáhá jako inspirace.
Stefan S
uživatel iOS
Tahle aplikace je fakt skvělá. Je tam tolik studijních poznámek a pomůcek [...]. Můj problémový předmět je například francouzština a aplikace nabízí tolik možností pomoci. Díky této aplikaci jsem si zlepšil francouzštinu. Doporučil bych ji každému.
Samantha Klich
uživatelka Androidu
Páni, jsem opravdu ohromen. Zkusil jsem aplikaci jen proto, že jsem ji mnohokrát viděl v reklamách, a byl jsem naprosto ohromen. Tato aplikace je TA POMOC, kterou chceš do školy, a především nabízí spoustu věcí, jako jsou cvičení a přehledy faktů, které mi osobně VELMI pomohly.
Anna
uživatelka iOS
Dříve jsem měl problémy s dokončováním úkolů včas, dokud jsem neobjevil Knowunity, který nejen usnadňuje nahrávání mého vlastního obsahu, ale také poskytuje skvělé shrnutí, díky kterým je moje práce rychlejší a efektivnější.
Thomas R
uživatel iOS
Vždy bylo výzvou najít všechny důležité informace pro mé úkoly – od té doby, co používám Knowunity, můžu jednoduše nahrát svůj obsah a těžit ze shrnutí ostatních, což mi hodně pomáhá s organizací.
Lisa M
uživatelka Androidu
Často jsem měl pocit, že nemám dostatečný přehled při učení, ale od té doby, co používám Knowunity, to už neplatí – nahraju svůj obsah a vždy najdu užitečná shrnutí na platformě, což mi učení značně usnadňuje.
David K
uživatel iOS
Ta aplikace je prostě skvělá! Stačí zadat téma do vyhledávání a dostanu odpověď opravdu rychle. Nemusím koukat na 10 YouTube videí, abych něčemu porozuměl, takže šetřím čas. Vřele doporučuji!
Sudenaz Ocak
uživatel Androidu
Ve škole mi matematika vůbec nešla, ale díky této aplikaci se mi teď daří lépe. Jsem moc vděčný, že jste tuhle aplikaci vytvořili.
Greenlight Bonnie
uživatel Androidu
Dřív bylo opravdu těžké shromáždit všechny informace na moje prezentace. Ale od té doby, co používám Knowunity, prostě nahraju svoje poznámky a najdu skvělé souhrny od ostatních – díky tomu je moje studium mnohem efektivnější!
Julia S
uživatelka Androidu
Byl jsem neustále ve stresu kvůli všem studijním materiálům, ale od té doby, co používám Knowunity, nahrávám svoje věci a koukám na super souhrny od ostatních – opravdu mi to pomáhá všechno lépe zvládat a je to mnohem méně stresující.
Marco B
uživatel iOS
TY KVÍZY A KARTIČKY SOU TAK UŽITEČNÝ A MILUJU Knowunity AI. JE TO TAKY DOSLOVA JAKO CHATGPT ALE CHYTŘEJŠÍ!! POMOHLO MI TO I S PROBLÉMY S ŘASENKOU!! A TAKY S MÝMA SKUTEČNÝMA PŘEDMĚTAMA! JASNÝ 😍😁😲🤑💗✨🎀😮
Sarah L
uživatelka Androidu
Dřív jsem trávil hodiny googlováním školních materiálů, ale teď prostě nahraju svoje věci na Knowunity a prohlížím si užitečné souhrny od ostatních – při přípravě na zkoušky se cítím mnohem jistější.
Paul T
uživatel iOS
Aplikace je velmi jednoduchá na používání a dobře navržená. Zatím jsem našel vše, co jsem hledal, a mohl jsem se z prezentací hodně naučit! Určitě použiju aplikaci na školní úkol! A samozřejmě taky hodně pomáhá jako inspirace.
Stefan S
uživatel iOS
Tahle aplikace je fakt skvělá. Je tam tolik studijních poznámek a pomůcek [...]. Můj problémový předmět je například francouzština a aplikace nabízí tolik možností pomoci. Díky této aplikaci jsem si zlepšil francouzštinu. Doporučil bych ji každému.
Samantha Klich
uživatelka Androidu
Páni, jsem opravdu ohromen. Zkusil jsem aplikaci jen proto, že jsem ji mnohokrát viděl v reklamách, a byl jsem naprosto ohromen. Tato aplikace je TA POMOC, kterou chceš do školy, a především nabízí spoustu věcí, jako jsou cvičení a přehledy faktů, které mi osobně VELMI pomohly.
Anna
uživatelka iOS
Dříve jsem měl problémy s dokončováním úkolů včas, dokud jsem neobjevil Knowunity, který nejen usnadňuje nahrávání mého vlastního obsahu, ale také poskytuje skvělé shrnutí, díky kterým je moje práce rychlejší a efektivnější.
Thomas R
uživatel iOS
Vždy bylo výzvou najít všechny důležité informace pro mé úkoly – od té doby, co používám Knowunity, můžu jednoduše nahrát svůj obsah a těžit ze shrnutí ostatních, což mi hodně pomáhá s organizací.
Lisa M
uživatelka Androidu
Často jsem měl pocit, že nemám dostatečný přehled při učení, ale od té doby, co používám Knowunity, to už neplatí – nahraju svůj obsah a vždy najdu užitečná shrnutí na platformě, což mi učení značně usnadňuje.
David K
uživatel iOS
Ta aplikace je prostě skvělá! Stačí zadat téma do vyhledávání a dostanu odpověď opravdu rychle. Nemusím koukat na 10 YouTube videí, abych něčemu porozuměl, takže šetřím čas. Vřele doporučuji!
Sudenaz Ocak
uživatel Androidu
Ve škole mi matematika vůbec nešla, ale díky této aplikaci se mi teď daří lépe. Jsem moc vděčný, že jste tuhle aplikaci vytvořili.
Greenlight Bonnie
uživatel Androidu
Dřív bylo opravdu těžké shromáždit všechny informace na moje prezentace. Ale od té doby, co používám Knowunity, prostě nahraju svoje poznámky a najdu skvělé souhrny od ostatních – díky tomu je moje studium mnohem efektivnější!
Julia S
uživatelka Androidu
Byl jsem neustále ve stresu kvůli všem studijním materiálům, ale od té doby, co používám Knowunity, nahrávám svoje věci a koukám na super souhrny od ostatních – opravdu mi to pomáhá všechno lépe zvládat a je to mnohem méně stresující.
Marco B
uživatel iOS
TY KVÍZY A KARTIČKY SOU TAK UŽITEČNÝ A MILUJU Knowunity AI. JE TO TAKY DOSLOVA JAKO CHATGPT ALE CHYTŘEJŠÍ!! POMOHLO MI TO I S PROBLÉMY S ŘASENKOU!! A TAKY S MÝMA SKUTEČNÝMA PŘEDMĚTAMA! JASNÝ 😍😁😲🤑💗✨🎀😮
Sarah L
uživatelka Androidu
Dřív jsem trávil hodiny googlováním školních materiálů, ale teď prostě nahraju svoje věci na Knowunity a prohlížím si užitečné souhrny od ostatních – při přípravě na zkoušky se cítím mnohem jistější.
Paul T
uživatel iOS